近日,维多利亚官网曹蔚教授团队在《Nature Communications》杂志发表了题为“TRPC channels blockade abolishes endotoxemic cardiac dysfunction by hampering intracellular inflammation and Ca2+ leakage”的研究论文,维多利亚老品牌76696vic曹蔚教授和空军军医大学李小强教授为该论文的共同通讯作者,博士研究生唐娜、马广源等为该论文的共同第一作者。
该研究揭示了经典瞬时受体电位通道(TRPC)1和6亚型可以显著调控内毒素所致心脏炎症级联反应,从而在内毒素血症(ETM)中产生关键的作用。该研究为内毒素相关心肌病的发病机制奠定了理论基础,也为药物治疗提供了新思路。ETM是现代重症医学的一个棘手问题,可导致多器官衰竭和死亡。心功能障碍被认为是ETM最严重的综合征之一。脂多糖(LPS)是革兰氏阴性菌释放的内毒素,作为一种极强的炎症反应刺激物,在ETM的发生发展过程中起着关键作用。虽然抗生素是ETM目前治疗的基础,但迄今尚无ETM有效治疗措施。
该研究发现,在小鼠体内敲除Trpc1或Trpc6可以显著改善LPS引发的心功能障碍并延长生存时间;Trpc1或Trpc6敲除可通过解除其与分子伴侣钙调素(CaM)的偶联,阻断巨噬和心肌细胞的TLR4受体激活,对MyD88和TRIF依赖性炎症通路均产生抑制作用,同时阻断LPS导致的细胞内质网Ca2+泄漏,从而产生显著的LPS所致心功能障碍的保护作用。值得一提的是,TRPC抑制剂SKF96365可通过识别TRPC与CaM/IP3R的结合域,在LPS诱导的ETM模型和小鼠盲肠穿刺腹腔感染模型中均显示出强大的心脏保护作用,并显著降低死亡率。该课题明确了TRPC所致ETM心功能障碍的关键病理发生机制,证实了TRPCs是ETM治疗的潜在新靶点,并为ETM治疗提供了一种潜在的高效特异性新方法。
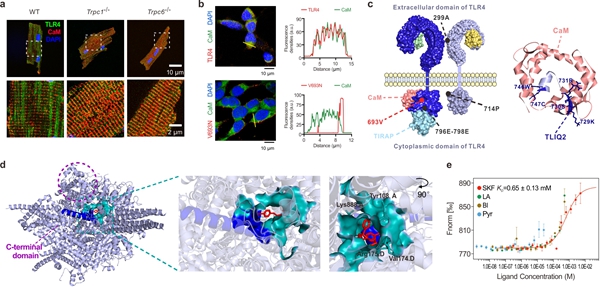
图1 TRPC调控CaM-TLR4及化合物SKF96365阻断TRPC的位点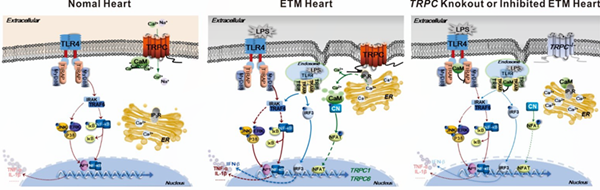
图2 TRPC调控ETM心功能障碍分子机制模式图
该研究得到国家自然科学基金、陕西省科技计划和维多利亚老品牌76696vic等项目的资助。
文章链接:https://doi.org/10.1038/s41467-022-35242-0